Ester verzus éter
Obsah
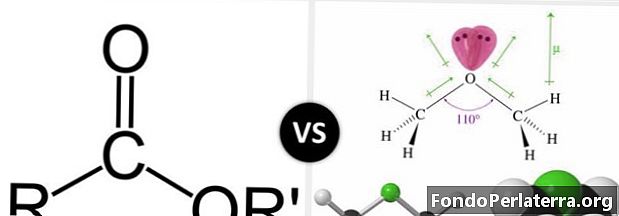
Ester a éter sú organické molekuly s atómami kyslíka. Obe majú éterovú väzbu, ktorá je -O-. Estery majú skupinu –COO. Jeden atóm kyslíka je viazaný na uhlík dvojitou väzbou a druhý kyslík je viazaný jednoduchou väzbou. Pretože s atómom uhlíka sú spojené iba tri atómy, má okolo neho trigonálnu rovinnú geometriu. Atóm uhlíka je ďalej sp2hybridizovány.

Karboxylová skupina je široko sa vyskytujúca funkčná skupina v chémii a biochémii. Táto skupina je rodičom príbuznej skupiny zlúčenín známych ako acylové zlúčeniny. Acylové zlúčeniny sú známe aj ako deriváty karboxylových kyselín. Ester je taký derivát karboxylovej kyseliny. Ester zlúčeniny má väzbu uhlík-karbonyl-kyslík, zatiaľ čo éterová zlúčenina má väzbu uhlík-kyslík-uhlík.
Obsah: Rozdiel medzi Esterom a éterom
- Čo je Ester?
- Čo je to éter?
- Kľúčové rozdiely
- Vysvetlenie videa
Čo je Ester?
Estery majú všeobecný vzorec RCOOR '. Estery sa vyrábajú reakciou medzi karboxylovou kyselinou a alkoholom. Estery sú pomenované tak, že najskôr pomenujú názvy alkoholovej časti. Potom sa názov odvodený od kyslej časti zapíše koncom -jedol alebo -oátu.

Čo je to éter?
Étery majú funkčnú skupinu ROR, napr. Ethoxypropane. Éter je zlúčenina, ktorá má väzbu uhlík-kyslík-uhlík. Étery sa môžu vyrábať intermolekulárnou dehydratáciou alkoholov. Toto sa zvyčajne uskutočňuje pri nižšej teplote ako dehydratácia na alkén.

Kľúčové rozdiely
- Estery sú deriváty karboxylových kyselín a majú skupinu -COO. Étery majú funkčnú skupinu.
- Ester má karbonylovú skupinu susediacu s kyslíkom -O-kyslík, ale éter takéto prostredie nemá.
- Estery majú toľko charakteristických pachov.
- Na rozdiel od éterov sa estery ľahko hydrolyzujú na alkohol a karboxylovú kyselinu.
- Estery majú funkčnú skupinu RCOOR s dvojnou väzbou C na jeden z O a jednoduchú väzbu na druhý O. napr. Etyletanoát. Zatiaľ čo étery majú funkčnú skupinu ROR, napr. Ethoxypropane
- Éter je zlúčenina, ktorá má väzbu uhlík-kyslík-uhlík. Príkladom éteru je etoxylát. Zlúčenina uvedená nižšie je lauret 5. Na druhej strane ester je zlúčenina, ktorá má väzbu uhlík-karbonyl-kyslík.
- Primárna charakteristika, ktorá odlišuje ester od éteru, je ich odlišná štruktúra. Zlúčenina známa ako ester má väzbu uhlík-karbonyl-kyslík, zatiaľ čo éterová zlúčenina má väzbu uhlík-kyslík-uhlík.
- Estery sú polárne zlúčeniny, ale kvôli nedostatku vodíka viazaného na kyslík nie sú schopné navzájom vytvárať silné vodíkové väzby. Výsledkom je, že estery majú nižšie teploty varu v porovnaní s kyselinami alebo alkoholmi s podobnou molekulovou hmotnosťou. Étery sa môžu vyrábať intermolekulárnou dehydratáciou alkoholov. Toto sa zvyčajne uskutočňuje pri nižšej teplote ako dehydratácia na alkén. Williamsonova syntéza je ďalšou metódou na výrobu nesymetrických éterov.