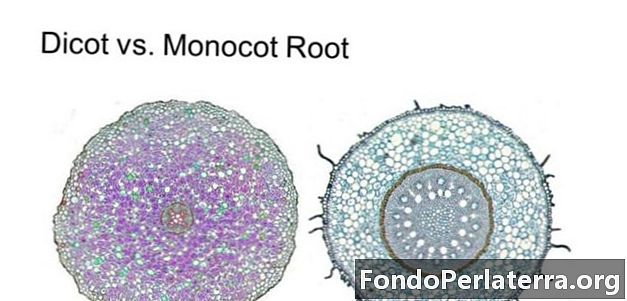
Reakcie SN1 vs. Reakcie SN2

Obsah
- Obsah: Rozdiel medzi reakciami SN1 a reakciami SN2
- Porovnávacia tabuľka
- Čo sú SN1 reakcie?
- Čo sú SN2 reakcie?
- Kľúčové rozdiely
Reakcie SN1 sú typom nukleofilnej substitúcie, ktorá sa vyskytuje vždy, keď krok určujúci rýchlosť vyžaduje iba jednu zložku. Reakcie SN2 sú typom nukleofilnej substitúcie, ktorá sa vyskytuje vždy, keď krok určujúci rýchlosť vyžaduje najmenej dva prvky. Počas tohto procesu sa jedna väzba zlomí a druhá sa vytvorí synchrónne.
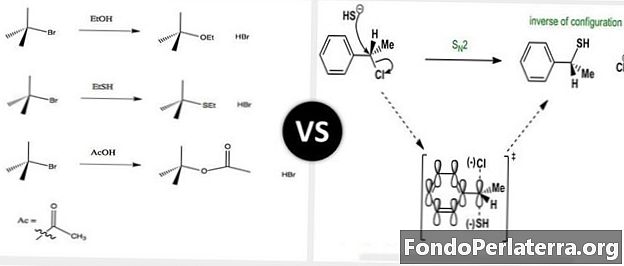
Obsah: Rozdiel medzi reakciami SN1 a reakciami SN2
- Porovnávacia tabuľka
- Čo sú SN1 reakcie?
- Čo sú SN2 reakcie?
- Kľúčové rozdiely
Porovnávacia tabuľka
| Základ rozlíšenia | Reakcie SN1 | Reakcie SN2 |
| definícia | Druh nukleofilnej substitúcie, ktorá sa vyskytuje vždy, keď krok určujúci rýchlosť vyžaduje iba jednu zložku. | Druh nukleofilnej substitúcie, ktorá sa vyskytuje vždy, keď krok určujúci rýchlosť vyžaduje najmenej dva prvky. Počas tohto procesu sa jedna väzba zlomí a druhá sa vytvorí synchrónne. |
| kroky | Počet krokov potrebných na dokončenie má niekoľko častí, ktoré sa začínajú odstránením opúšťania skupiny a potom útočia na nukleofil. | Väčšina výsledkov v rámci procesu sa dokončí iba v jednom kroku a koncentrácia nukleofilu sa stáva kritickou. |
| požiadavka | Slabý nukleotid | Silný nukleotid |
| príroda | Unimolekulárna entita, a preto dostane názov reakcie prvého poriadku. | bimolekulárna reakcia, a preto má názov reakcia druhého poriadku. |
| etapy | Raz cyklus s dvoma medzistupňami. | Dva cykly s jedným medzistupňom. |
Čo sú SN1 reakcie?
Reakcie SN1 sú typom nukleofilnej substitúcie, ktorá sa vyskytuje vždy, keď krok určujúci rýchlosť vyžaduje iba jednu zložku. SN1 reakcia je substitučná reakcia v prírodných vedách. „SN“ zostáva pre nukleofilnú substitúciu a „1“ hovorí o tom, že krok rozhodujúci o rýchlosti je neimolekulárny. Týmto spôsobom sa pomer rýchlosti pravidelne javil ako závislý na elektrofile v prvom rade a na nukleofilnom usporiadaní s nulovým usporiadaním. Tento vzťah platí za okolností, keď je miera nukleofilu výrazne výraznejšia ako miera karbokacie na polceste. Skôr môže byť pomer rýchlosti ešte presnejšie vykreslený pomocou stálej energie štátu. Odpoveď zahŕňa karbolačný stred cesty a pravidelne sa vyskytuje v odpovediach prípadných alebo terciárnych alkylhalogenidov za pevne základných podmienok alebo za jednoznačne kyslých podmienok s pomocnými alebo terciárnymi alkoholmi. S esenciálnymi a voliteľnými alkylhalogenidmi nastáva možnosť SN2 reakcie. V chemickej vede je odpoveď SN1 pravidelne známa ako disociačný systém. Cislový náraz všade zobrazuje túto separačnú cestu. Nástroj reakcie bol prvýkrát navrhnutý Christopherom Ingoldom a kol. v roku 1940. Táto reakcia veľmi nezávisí od kvality nukleofilu, vôbec nie od nástroja SN2. V SN1 reakcii je krokom rozhodujúcim o rýchlosti strata zvyšujúceho sa zhromaždenia, aby sa vytvoril stred cestnej karbonácie. Čím je karbocation stabilnejší, tým je jeho tvar ľahší a rýchlejšia bude odpoveď SN1. Niekoľko mienkotvorcov sa dostane do pasce viery, že rámec s menej stabilnou karbonatáciou bude reagovať najrýchlejšie. Avšak prehliadajú, že rozhoduje o dobe karbocation.
Čo sú SN2 reakcie?
Reakcie SN2 sú typom nukleofilnej substitúcie, ktorá sa vyskytuje vždy, keď krok určujúci rýchlosť vyžaduje najmenej dva prvky. Počas tohto procesu sa jedna väzba zlomí a druhá sa vytvorí synchrónne. Reakcia SN2 je akýmsi nástrojom reakcie, ktorý je v prírodovednom odbore zásadný. V tejto zložke je jedna väzba prerušená a jeden vzťah je orámovaný synchrónne, t.j. v jednej fáze. SN2 je druh nástroja nukleofilnej substitučnej reakcie. Pretože dva reagujúce druhy zahrnuté v miernom (rýchlosť rozhodujúcom) kroku, vyvoláva to výraz substitučný nukleofilný (dvojväzbový atóm) alebo SN2; ďalším významným druhom je SN1. Odpoveď na zmenu je znázornená na mnohých ďalších konkrétnych nástrojoch. K prerušeniu väzby C – X a rozvoju nového vzťahu (pravidelne označovaného ako C – Y alebo C – Nu) dochádza súčasne s pohyblivým stavom, v ktorom je uhlík pod nukleofilným útokom pentacoordinate a zhruba sp2 hybridizovaný. Nukleofil útočí na uhlík pri 180 ° k odchádzajúcemu zhromaždeniu, pretože to poskytuje najlepšie krytie medzi jednoduchou zhodou nukleofilného vlákna a protiväzbovým orbitálom C – X σ *. Odchádzajúca zbierka potom vytlačila opačnú stranu a predmet sa zarámuje obrátením tetrahedrálnej geometrie v ohniskovej iote. Substrát má najkritickejší vplyv pri rozhodovaní o rýchlosti reakcie. Stáva sa to kvôli útokom nukleofilov zo zadnej strany substrátu, pozdĺž týchto línií, ktoré porušujú uhlíkovú skupinu odchádzajúcu uhlík a formujú uhlíkovú nukleofilnú bezpečnosť.
Kľúčové rozdiely
- Reakcie SN1 sú typom nukleofilnej substitúcie, ktorá sa vyskytuje vždy, keď krok určujúci rýchlosť vyžaduje iba jednu zložku. Na druhej strane SN2 reakcie sú typom nukleofilnej substitúcie, ktorá sa vyskytuje vždy, keď krok určovania rýchlosti vyžaduje najmenej dva prvky. Počas tohto procesu sa jedna väzba zlomí a druhá sa vytvorí synchrónne.
- Počet krokov potrebných na dokončenie reakcie SN1 má niekoľko častí, ktoré začínajú odstránením opúšťajúcich skupinu a potom atakujú nukleofil. Na druhej strane, väčšina výsledkov v procese SN2 je ukončená v jedinom kroku a koncentrácia nukleofilu sa stáva kritickou.
- Požiadavka na SN1 reakcie sa stáva požiadavkou slabých nukleofilov, pretože majú prirodzenú tendenciu neutralizovať rozpúšťadlá. Na druhej strane, dopyt po reakciách SN2 sa stáva dopytom po silných nukleofiloch, pretože majú negatívny náboj.
- Povaha SN1 reakcie sa stáva povahou neimolekulárnej entity, a preto dostane názov reakcie prvého poriadku. Na druhej strane sa povaha SN2 reakcie stáva povahou bimolekulárnej reakcie, a preto sa nazýva reakcia druhého poriadku.
- Reakcie SN1 sú ukončené v jednom úplnom cykle, ktorý má dva medzistupne. Na druhej strane reakcia SN2 končí v jednom cykle, ktorý má len jediný medzistupeň.